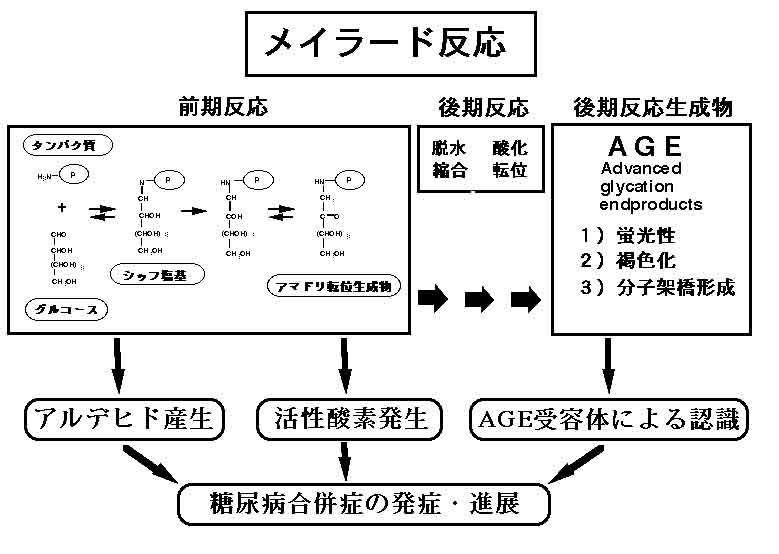

メイラード反応は前期及び後期反応に分けることができます。前期反応では、還元糖のアルデヒド基がN末端アミノ基や、リジン残基のε-アミノ基と反応してシッフ塩基を形成した後、1,2-エナミノールを経てアマドリ転位産物を生成します。これらの前期反応生成物は、酸化・脱水・縮合などの複雑な反応を経て褐色化・蛍光・架橋形成などの物理化学的特徴、又、AGE受容体によってリガンドとして認識されるという生物学的特徴を有するAGE構造体へと変化します。即ち、AGEとは前期反応生成物が複雑な反応を経て不可逆的に生成された構造体の総称であり、現在、生体に存在するAGE構造として蛍光性・架橋性を有するペントシジン、クロスリン、又、非蛍光性・非架橋性のイミダゾロン、カルボキシメチルリジン(CML)やピラリンなどが知られています(既知AGE構造体の項参照)。
メイラード反応は還元糖のアルデヒド基とタンパク質のアミノ基との非酵素的な反応が初期段階であるため、グルコースに限らずアルデヒド基を有する物質であれば同様な反応が進行します(Nagai R et al., Diabetes 49, 1714-1723, 2000)。当初、生体におけるメイラード反応は主にグルコースと蛋白との反応であると考えられていましたが、最近ではグルコースの自己酸化、脂質の過酸化、細胞内の糖代謝などからグルコースに比較して高い反応性を示すグリオキサール、メチルグリオキサール、グリコールアルデヒド(GA)、3-デオキシグルコソン、グルコソン等のアルデヒドが蛋白のAGE化に深く関与していることが知られています。例えばメチルグリオキサールは細胞内で解糖系およびポリオール経路からも生成し、I型糖尿病患者の血中メチルグリオキサール含量は正常者の6倍、硝子体では2倍程度増加することが報告されています。
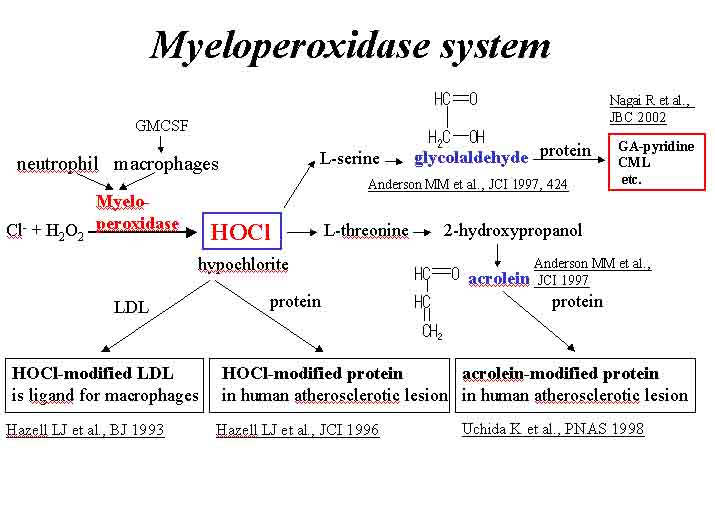
又、我々は、活性化されたリンパ球系細胞はミエロペルオキシダーゼの発現を介してGAを産生し、さらにGAはリジンと不可逆的に反応してAGE構造体であるGA-pyridineを生成することを報告しました(上図)(Nagai R et al., J Biol Chem 277, 48905-48912, 2002)。GA-pyridineは動脈硬化巣の泡沫化マクロファージ内に顕著に蓄積していることから、動脈硬化の進展にはGAによる蛋白の修飾も関与していると考えられます。従って、持続する高血糖状態は酸化ストレス、炎症、糖代謝の異常などから上述した反応性の高いアルデヒドの産生が亢進されることから、結果的に蛋白の修飾・変性が促進される状況であると言えるでしょう。なお、アルデヒドに存在するカルボニル基(C=O)が蛋白との反応部位であることから、アルデヒドによる生体蛋白の修飾は、カルボニルストレスとも言われています。
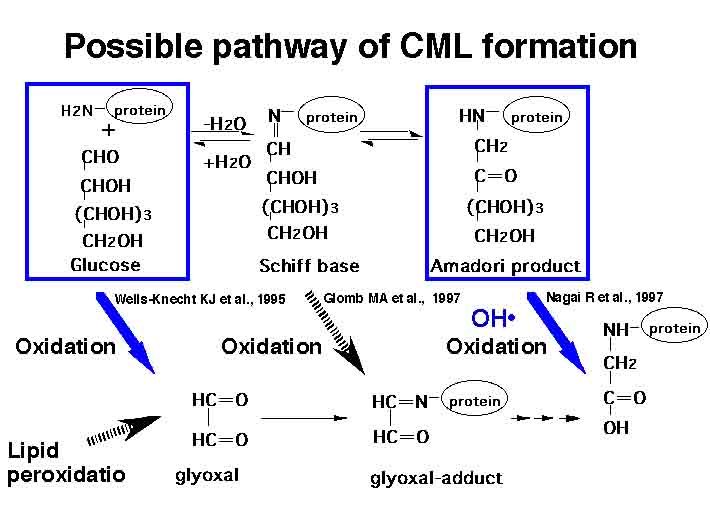
主要なAGE構造体として報告されているCMLは、(1) アマドリ転位物の開裂(Nagai
R et al., Biochem Biophys Res Commun 234, 167-172, 1997)、(2) シッフ塩基の開裂、(3)
グルコースの自己酸化によってグリオキサールを介した経路、さらには(4) 脂質の過酸化反応によってグリオキサールを介した経路(左図)からも生成することが明らかとなっていますが、いずれの経路においてもCMLの生成には酸化反応が必須であることが明らかとなっており、CMLは特に生体における酸化反応のマーカーとして捉えられています。
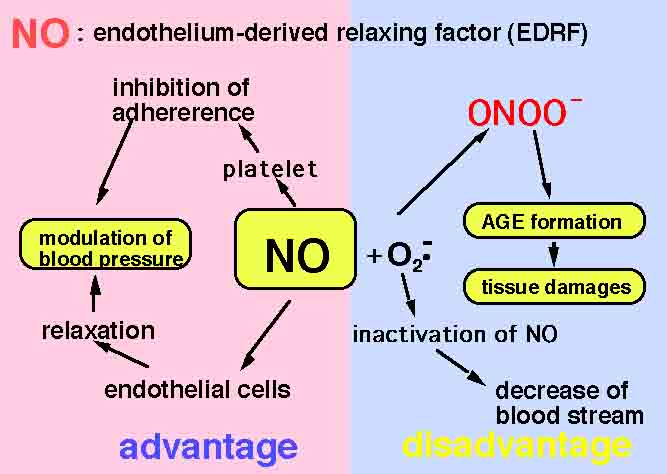
又、メイラード反応による糖尿病合併症の発症機構については、血管弛緩因子として知られる一酸化窒素(NO)との関与も考えられます。血管内皮細胞におけるNO合成酵素の転写調節にはインスリンが関与しており、インスリン欠乏下ではNO合成酵素活性が低下していることが知られています。さらに、炎症細胞、あるいはアマドリ転位物から発生したO2-はNOと迅速に反応してNOを消去します。したがって、インスリン欠乏による持続的な高血糖状態は、(1)
メイラード反応の亢進によるO2-の産生増加、(2) O2-によるNO分解の亢進、(3) NO産生の減少による血管拡張能の異常が引き起こされます(左図)。また、NOとO2-の反応によってより酸化能の強いペルオキシナイトライト(ONOO-)が生成しますが、ONOO-によって脂質の過酸化反応は更に促進され、さらに、我々はONOO-が単に蛋白を酸化するのみならず、前期中間体であるアマドリ転位物に作用するとAGE生成を促進することを明らかにしました(Nagai
R et al., Diabetes 51, 2833-2839, 2002)。本現象は、糖尿病合併症の発症要因の一原因と考えられております。