研究内容
ミカヅキモの有性生殖機構の解析
有性生殖は、現在の生物の繁栄、多様性に密接な関わりをもつ根本的・基礎的な現象である。その成否は、生物種を問わず、最終的には二個の配偶子細胞間での情報交換に依存する。この問題に取り組むにあたり、陸上植物と非常に近縁な単細胞接合藻ミカヅキモを主に用いてきた。この材料は、遺伝的に異なる+型及び−型細胞の間で有性生殖を行い、最終的に接合子を形成する。これまでに、ミカヅキモの有性生殖に関わる性フェロモンの発見を足がかりにして、細胞間で行われる情報交換を生理学的、生化学的、分子生物学的に解析してきた。
1)ヒメミカヅキモ(Closterium peracerosum-strigosum-littorale complex)の性フェロモンの解析
ヒメミカヅキモの有性生殖に関わる二種類の性フェロモン(PR-IP および PR-IP Inducer)を発見し、精製することに成功した(Sekimoto et al. 1990, 1993a; Nojiri et al. 1995)。さらに、PR-IPは配偶子嚢細胞へと分化した−型細胞の細胞膜受容体に結合して作用することを実証した(Sekimoto et al. 1993b; Sekimoto & Fujii 1992)。また、それぞれの性フェロモンをコードするcDNA及びゲノムDNAを単離し、有性生殖プログラムの一端を明らかにした(Endo et al. 1998; Sekimoto 2000; Sekimoto et al. 1994a,b,c, 1998)。
さらに、両接合型細胞のSCDを誘起する二種類の性フェロモンを見出した(Tsuchikane et al. 2003)。また、有性生殖時には、細胞外への不溶性多糖分泌が顕著に促進されるが、この促進活性を持つ性フェロモン(MS-IP)二種類をも見出した(Akatsuka et al. 2003)。これらの新規の生理活性物質の精製を進めた結果、既知の性フェロモンであるPR-IP, PR-IP Inducer自身が活性の本体であり、作用機構が異なることが強く示唆された(Tsuchikane et al. 2005; Akatsuka et al. 2006)。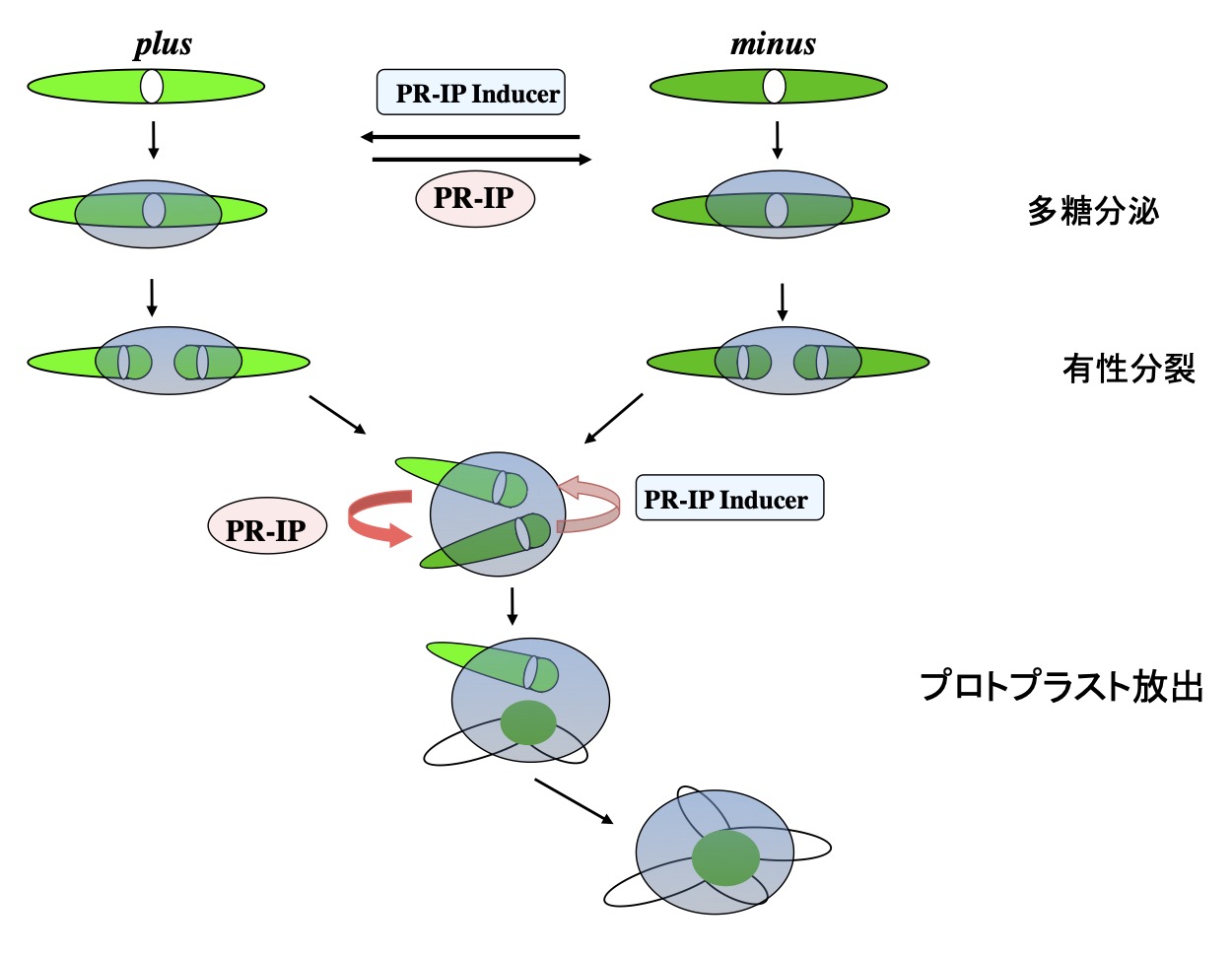
2)ヒメミカヅキモの有性生殖に関わる遺伝子群の網羅的解析
ヒメミカヅキモの有性生殖、無性生殖期より均一化cDNAライブラリーを構築し、これまでに3200を超えるEST情報を得た。さらにそれらをもとにして、cDNAマイクロアレイを作成し、+型または−型の配偶子嚢細胞への分化、有性生殖過程、性フェロモン処理に関わる88種のcDNA群を選別した(Sekimoto et al. 2003, 2006)。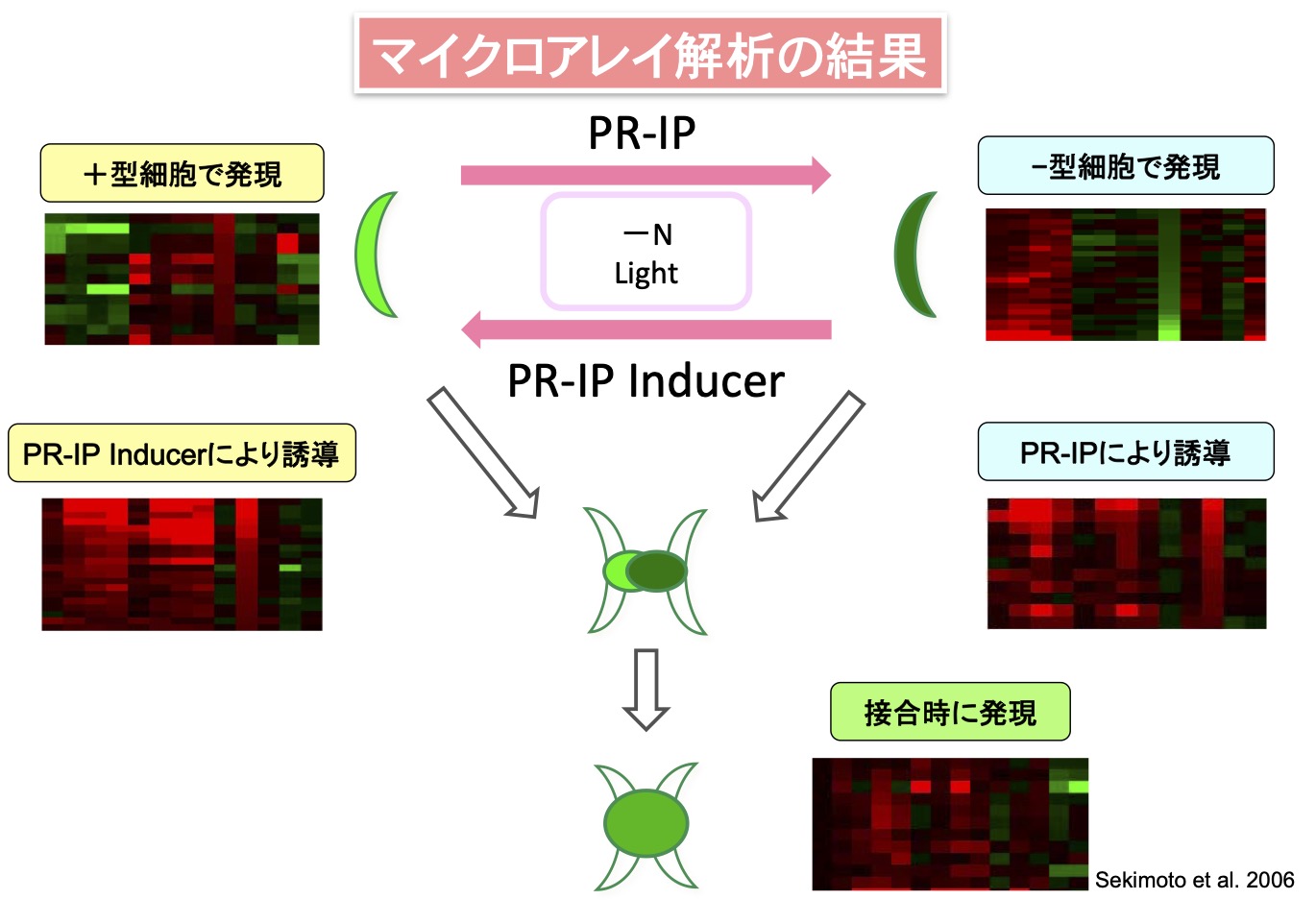
3)ヒメミカヅキモへの遺伝子導入系開発
マイクロアレイで見出した遺伝子群が、ヒメミカヅキモの有性生殖過程でどのような役割を果たしているのか、その詳細を明らかにするためには、RNAiなどによる遺伝子機能解析やGFPによるタンパク質局在解析が必要とされる。その前提となる、ヒメミカヅキモへの外来遺伝子導入条件について検討を進めた。
まず、ヒメミカヅキモゲノムから有性生殖過程で恒常的に強く発現している2種類の遺伝子(HSP70, CAB)のプロモーター領域を単離し、GFP遺伝子をレポーターとして結合したコンストラクトを作製した。パーティクルガンにより細胞に導入したところ、いずれのプロモーターでも導入後48〜72時間でGFPの一過的な発現が確認できた。次に核局在性の選択マーカー遺伝子(ble)をGFP遺伝子(cgfp)とインフレームで結合し導入したところ、核において強い蛍光が確認されたことから、本実験系がGFP融合タンパク質による細胞内局在解析にも適応しうる事が示された(Abe et al. 2008)。さらに、選択マーカー遺伝子 (ble, Hyg)を用いて、核ゲノム内に安定して遺伝子が取り込まれた形質転換株の確立にも成功し(Abe et al. 2011)、現在では、エレクトロポレーションにより、パーティクルガンの約100倍の高効率で、形質転換ヒメミカヅキモの確立が可能となった(Kawai et al. 2022)。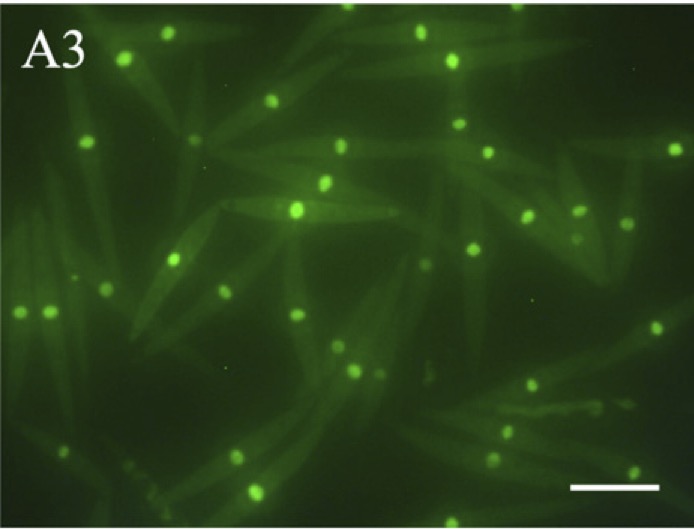
4)ヒメミカヅキモの有性生殖に関わるCpRLK1遺伝子の解析
マイクロアレイで見出された遺伝子群のうち、PR-IP Inducerに反応して+型細胞においてのみ発現する受容体型タンパク質リン酸化酵素(CpRLK1)をコードする遺伝子に注目した。
CpRLK1は、有性生殖時にペアを形成した一方の細胞の接合突起上に存在していることが、間接蛍光抗体法によって確認された。さらに、CpRLK1遺伝子をアンチセンスRNAによりノックダウンさせるためのコンストラクト(CpHSP70p::anti-CpRLK1-ECD)を作製し、本来これらの遺伝子が発現するはずの+型細胞に導入し、発現抑制を起こした形質転換株を作出したところ、両性のペアまでは形成するものの、プロトプラストの放出を起こさず、それ以上の接合過程に進行しないことが判明した(Hirano et al. 2015)。
CpRLK1は、細胞壁のセンサーとして機能すると考えられているCrRLK1L-1サブファミリーに含まれることが示され、接合時の細胞壁の状態をモニターし浸透圧調節をすることで、適切に細胞質の凝縮、プロトプラスト放出を促していることが示唆された。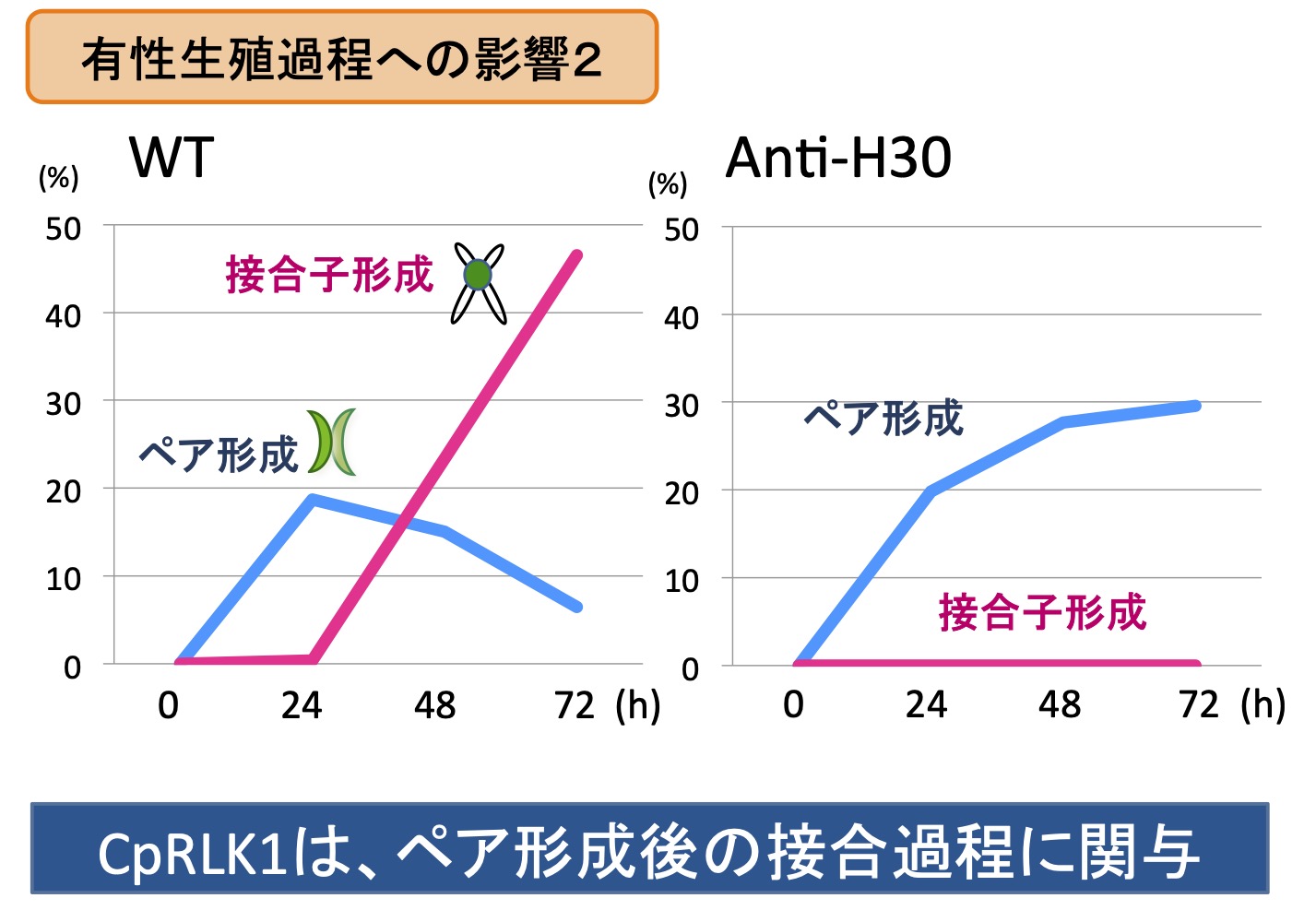
5)CRISPR/Cas9による遺伝子破壊法の確立
ヒメミカヅキモのゲノムに含まれる、有性生殖関連遺伝子、発生調節にかかわると推定される重要な遺伝子などの機能を逆遺伝学的に解析するために、CRISPR/Cas9による遺伝子破壊法の確立を目指した。まず、クラミドモナス用にコドン頻度を合わせたCas9遺伝子を譲り受け、発現ベクターであるpSA0104のもつHsp70遺伝子プロモーターの下流に連結した(pSA009104)。さらにヒメミカヅキモのゲノムより、U6 snRNAをコードする遺伝子を見出し、そのプロモーター領域をguide RNA scaffoldの上流側に連結するようにpSA009104に挿入し、pSA6009104ベクターを構築した。標的として、以下に示すCpRLP1遺伝子の2箇所の配列を選び、その遺伝子破壊に成功した(Kanda et al. 2017)。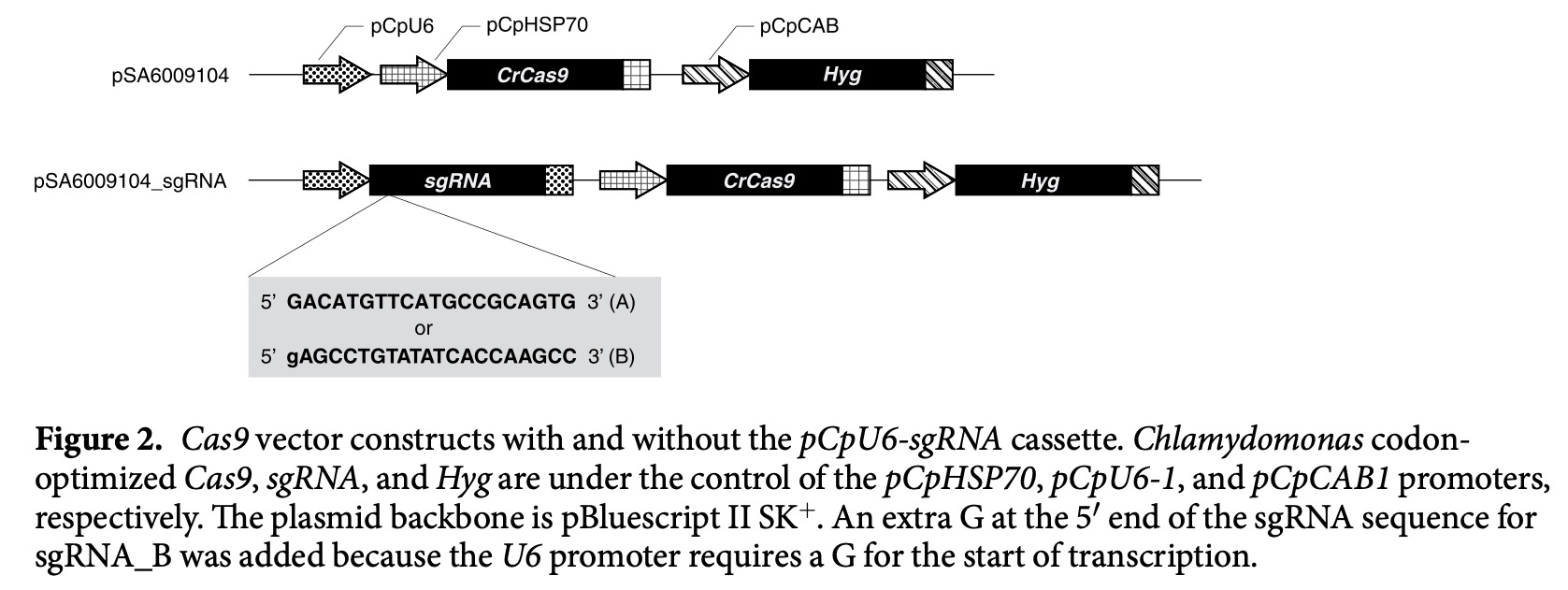
6)ヒメミカヅキモの有性生殖に関わるCpRLP1遺伝子の機能解析
CpRLP1は、PR-IPに反応して−型細胞においてのみ発現する、ロイシンリッチリピートを持つ受容体型タンパク質(CpRLP1)をコードする遺伝子であり、マイクロアレイで見出されていたがその機能は不明であった。
CRISPR/Cas9システムの導入によるCpRLP1遺伝子の破壊を試みたところ、得られた複数の形質転換体で、PAM配列の3塩基上流に変異が見られ、フレームシフトが引き起こされた。これらのCpRLP1遺伝子破壊株(CpRLP1-KO)と野生型の+型細胞を混合したところ、ペアを形成して接合に至る割合が顕著に減少し、単独でプロトプラスト放出する細胞が多く見られた。この際、タンパク質の発現は完全に失われたことが確認された。さらに、CpRLP1-KOは、PR-IPに対する反応性が非常に高まっていた。以上より、PR-IPにより誘導されたCpRLP1タンパク質がPR-IP受容のネガティブレギュレーターとして働くことで、ヒメミカヅキモの接合過程が制御されることが示唆された。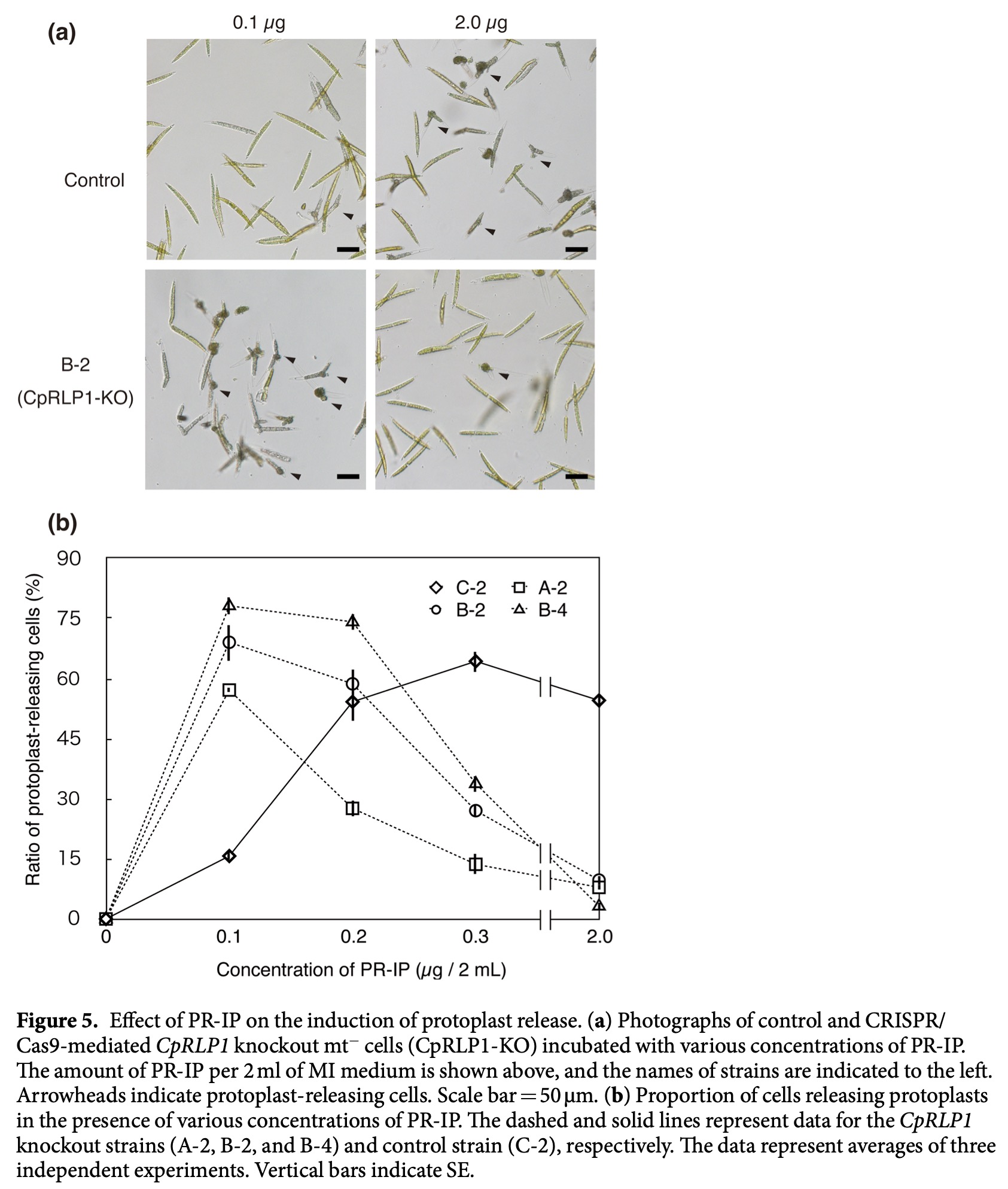
7)ヒメミカヅキモの有性生殖に関わるCpRLK2遺伝子の機能解析
CpRLP1遺伝子は、細胞内にキナーゼドメインを欠く受容体型タンパク質をコードしていた。また、CpRLP1と類似の細胞外ドメインを持つ受容体型キナーゼをコードするCpRLK2遺伝子が発見された。そこで、CpRLK2遺伝子破壊株 (CpRLK2-KO)を作出し、その表現型を調べたところ、CpRLK2-KOは、全く接合反応を示さず、PR-IPに対する反応性を失っていた。さらにこの変異株では、CpRLP1遺伝子の発現は見られなかった。以上より、CpRLK2タンパク質がPR-IP受容体であり、PR-IPにより誘導されたCpRLP1タンパク質とともに、ヒメミカヅキモの接合過程を精妙に制御していることが示唆された。
8)ヒメミカヅキモのゲノム解読
ヒメミカヅキモの+型株(NIES-67)および−型株(NIES-68)のそれぞれからゲノムDNAを抽出し、Illumina, PacBioなどの次世代、第三世代シークエンサーを用いたゲノム解読を進めている。
PacBioRSIIデータ(+型、−型とも23セル分、30xゲノムに相当)を用いて、バージョンアップしたFALCONによる解析を行ったところ、Contig N50が275-351 kb(contig数は約2500)となった。さらに、既存のRNA-seq, 完全長EST, Iso-seqの各データを教師データとして利用し、遺伝子アノテーションを進め、+型、−型のゲノムから、それぞれ25752,24985のタンパク質をコードする遺伝子を同定した。
9)ヒメミカヅキモの性決定機構の解析
ヒメミカヅキモの両ゲノム配列を比較し、−型ゲノムに特異的に存在するCpMinus1遺伝子を発見した。この遺伝子を+型で異所的に発現させると、形質転換体は−型としての性を示した。また、−型に存在する遺伝子を破壊すると、遺伝子破壊株は+型としての性表現を示した。以上から、この遺伝子がヒメミカヅキモの性決定にかかわるマスター遺伝子であることが強く示唆された。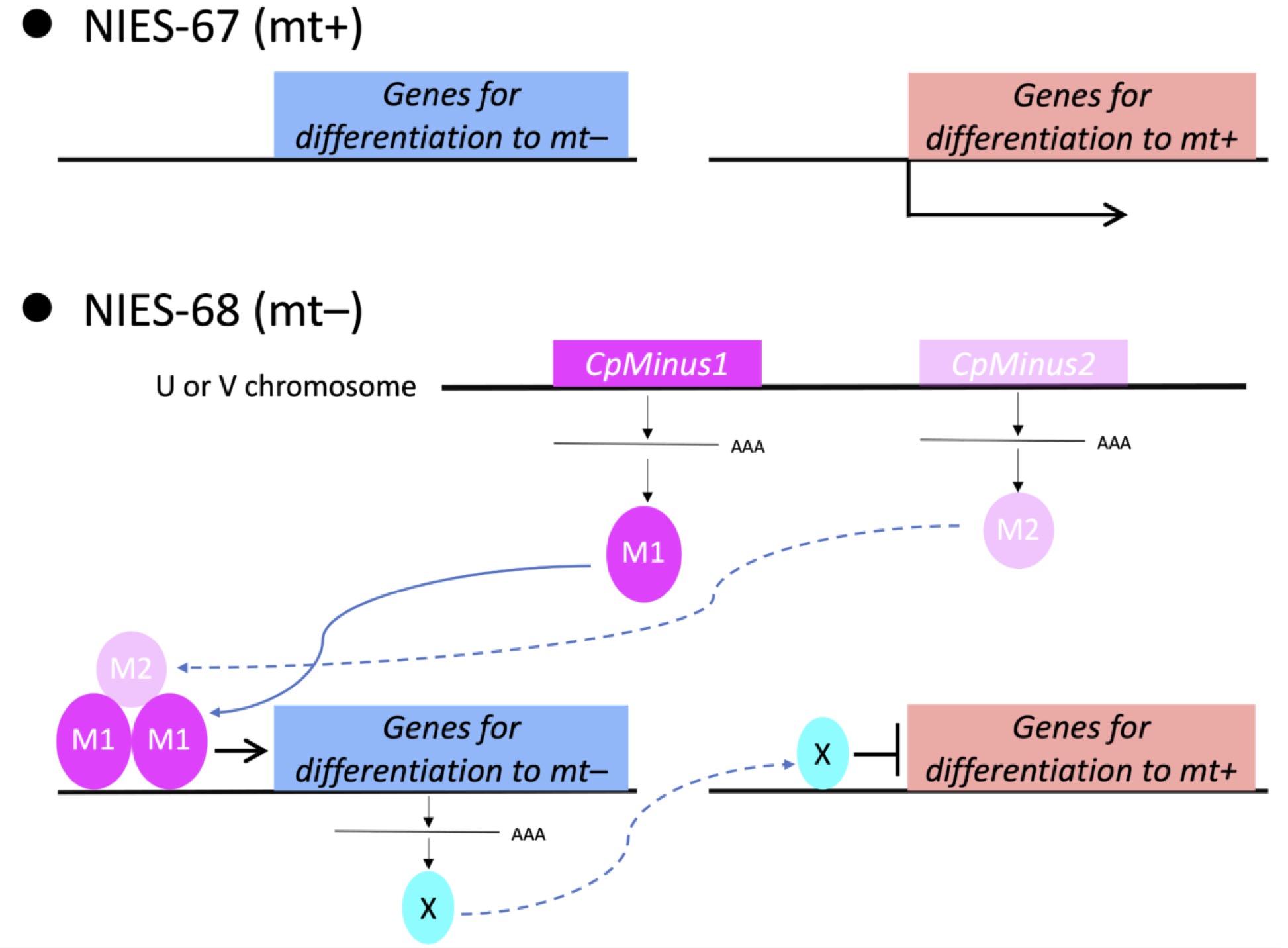 この研究の内容は、英国の国際科学雑誌New Phytologistに掲載されました。
この研究の内容は、英国の国際科学雑誌New Phytologistに掲載されました。
プレスリリース記事へ